 Jovem Pan News
Jovem Pan News
Jovem Pan News
No início desta semana, o Ministério da Saúde anunciou a compra de 46 milhões de doses da CoronaVac, vacina produzida pela farmacêutica chinesa Sinovac, em parceria com o Instituto Butantan, em São Paulo. Menos de 24 horas após essa sinalização da pasta, o presidente Jair Bolsonaro se pronunciou, dizendo que a vacina “não seria comprada”. O assunto gerou um mal-entendido entre o mandatário e o ministro da Saúde, Eduardo Pazuello, e fez com que o ministério voltasse atrás na decisão. “Um manda e o outro obedece”, afirmou Pazuello em vídeo gravado com Bolsonaro. Outra polêmica girou em torno da obrigatoriedade da imunização. Após Bolsonaro garantir que, “no seu governo, a vacinação não seria compulsória”, o ministro do Supremo Tribunal Federal (STF), Ricardo Lewandowski, decidiu nesta sexta-feira, 23, que vai levar para análise do plenário da Corte as ações que discutem o tema. Segundo o cronograma divulgado pelo Ministério da Saúde, a vacinação contra a Covid-19 deve acontecer somente no mês de abril de 2021, após todas as três etapas terem sido concluídas, e a Anvisa liberado a produção do imunizante no País.
O desenvolvimento de medicamentos e vacinas passa, no geral, por três fases: os estudos pré-clínicos (testes em animais e laboratório), os estudos clínicos (feitos com humanos) e o registro. No Brasil, quatro vacinas já foram autorizadas para desenvolvimento pela Agência Nacional de Vigilância Sanitária (Anvisa), a CoronaVac, a de Oxford, a da Pfizer + BioNTech, e a da Johnson & Johnson, sendo que as duas primeiras já estão em processo de análise final pelo mesmo órgão. Tendo em vista a urgência da situação por causa da pandemia da Covid-19, a agência regulatória definiu um novo procedimento para tornar mais rápida a análise de dados referente aos imunizantes: a submissão contínua. Ou seja, ao invés de aguardar o pedido de registro para receber toda a informação, as empresas vão enviando os dados conforme eles são gerados, o que economiza tempo. “Porém, as exigências técnicas em relação às vacinas não mudam, e não há redução de nenhum requisito de segurança e eficácia”, afirmou a agência em nota enviada à Jovem Pan.
Depois de realizadas as fases 1, 2 e 3 e, caso os resultados sejam favoráveis, as empresas responsáveis pelos imunizantes precisam enviar uma série de documentos técnicos e regulatórios, como os estudos detalhados destas três etapas, para que a Anvisa verifique os dados de segurança e eficácia, bem como avalie a qualidade da vacina. O registro, concedido pela agência regulatória, é o sinal verde para que o imunizante seja comercializado e disponibilizado no Brasil. Vale ressaltar que, quando o desenvolvimento clínico de uma vacina é inteiramente conduzido no exterior, não há a obrigatoriedade da anuência prévia, por parte da Anvisa, aos estudos clínicos. Porém, o registro permanece sendo necessário. De acordo com a Anvisa, para avaliação das propostas de estudo, e eventual registro de vacinas contra a Covid-19, “foi instituído um comitê de especialistas composto por 10 profissionais rotativos. Dessa forma, as responsabilidades são compartilhadas e as decisões podem ser tomadas com mais segurança. Essa equipe multidisciplinar – formada por farmacêuticos, médicos, biólogos e estatísticos – avalia os quatro aspectos de forma minuciosa e, ao mesmo tempo, célere”. Todos os profissionais que fazem essas análises têm, no mínimo, 10 anos de experiência na avaliação de protocolos de estudo e registro de vacinas.
Considerando os procedimentos específicos por causa da pandemia, a Anvisa definiu prazos de 72 horas para análise de autorização de pesquisa, e de 60 dias para análise do registro. Porém, o tempo de condução dos estudos depende de outros fatores, como a própria capacidade dos laboratórios e os resultados encontrados. Ou seja, não está sob controle da agência regulatória, e sim dos patrocinadores da pesquisa. O infectologista do hospital Beneficência Portuguesa de São Paulo, João Prats, explica que não é necessário terminar a fase 3 para que os dados sejam revisados. Porém, depois do registro, ainda é preciso começar a produção e a distribuição do imunizante, que pode ser facilitado nas vacinas que estão com parcerias em laboratórios brasileiros, como a CoronaVac e a vacina de Oxford. Entretanto, as instituições brasileiras precisam de autorização da Anvisa para a importação da matéria-prima para o início da fabricação local das vacinas, o que também pode levar tempo. “Preocupa porque a demanda é mundial. Teremos que esperar para ver como vai funcionar isso aqui no Brasil. Somos capazes de aumentar muito a nossa produção, mas a demanda é mundial”, afirma Prats. O especialista diz, ainda, que, durante a testagem, pode ocorrer “um dano muito grande, ou um benefício muito grande no grupo, que recebeu o imunizante”. Se for um dano, a pesquisa precisará ser interrompida para análises mais aprofundadas; se for um benefício, as pessoas que receberam o placebo também precisarão tomar uma dose, por uma “questão ética”.
A data ainda é incerta, já que até o momento nenhuma vacina foi aprovada no País. Para o infectologista João Prats, “boa parte dos estudos de fase 3 no Brasil devem acabar até o final do ano”. Depois disso, ainda é necessário conseguir o registro da Anvisa e começar a produção e distribuição do imunizante. A vacina mais avançada atualmente no Brasil é a CoronaVac, desenvolvida pelo laboratório chinês Sinovac, em parceria com o Instituto Butantan, em São Paulo. O governador do Estado, João Doria, disse que já enviou para a Anvisa os resultados finais dos testes em humanos , e que prevê que, se tudo der certo, o começo da vacinação para profissionais da área da saúde aconteça já em 15 de dezembro.
O Programa Nacional de Imunizações, criado em 1973 no Brasil e que faz parte do Sistema Único de Saúde (SUS), prevê a oferta gratuita de todas as vacinas que estão dentro do calendário brasileiro de vacinação. Ou seja, se o imunizante da Covid-19 entrar nesse programa, será oferecida sem custo. De acordo com o Ministério da Saúde, os primeiros a tomar a vacina serão as pessoas dos grupos de risco da Covid-19 e os profissionais da saúde, que ficam mais expostos ao vírus. São considerados grupo de risco para a doença os portadores de doenças crônicas – como diabetes e hipertensão, asma e doença pulmonar obstrutiva crônica –, as pessoas acima de 60 anos, além das gestantes e das puérperas.
Até agora, duas vacinas tiveram os testes interrompidos devido a efeitos adversos: a de Oxford e a da Johnson & Johnson. No caso da primeira, as análises foram retomadas logo depois no Reino Unido e nem chegaram a ser interrompidos no Brasil. Já em relação à segunda, os estudos foram parados no último dia 13, e os pesquisadores ainda aguardam uma investigação de maior profundidade do Comitê Independente de Segurança. O infectologista João Prats, explica que essas interrupções são chamadas de “evento sentinela”. “Quando você cria o estudo, você prevê que pode ter um caso de A, B, C, D, em que o estudo precisará ser parado para analisar. É por segurança, às vezes a gente aqui de fora nem fica sabendo. A de Oxford parou por um evento sentinela, o que significa que precisa parar e olhar. Se estiver tudo certo, continua”, afirma. Nesta quarta-feira, 21, um voluntário que participava das pesquisas da vacina AstraZeneca/Oxford contra o novo coronavírus morreu. No entanto, foi confirmado depois que ele estaria no grupo que recebeu o placebo.
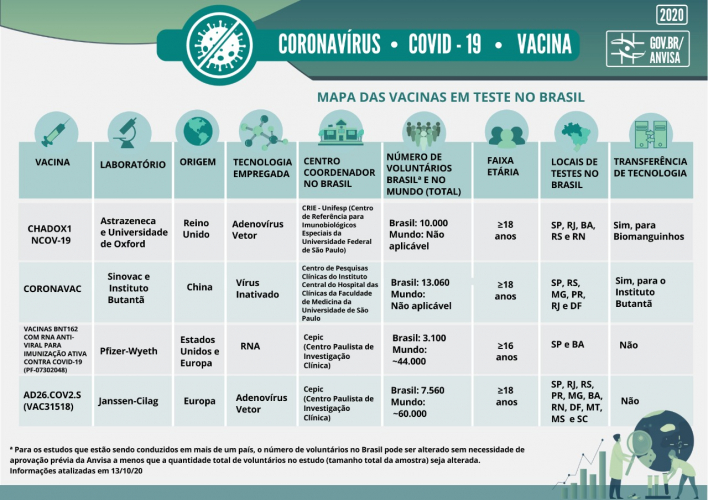
Reprodução/Anvisa